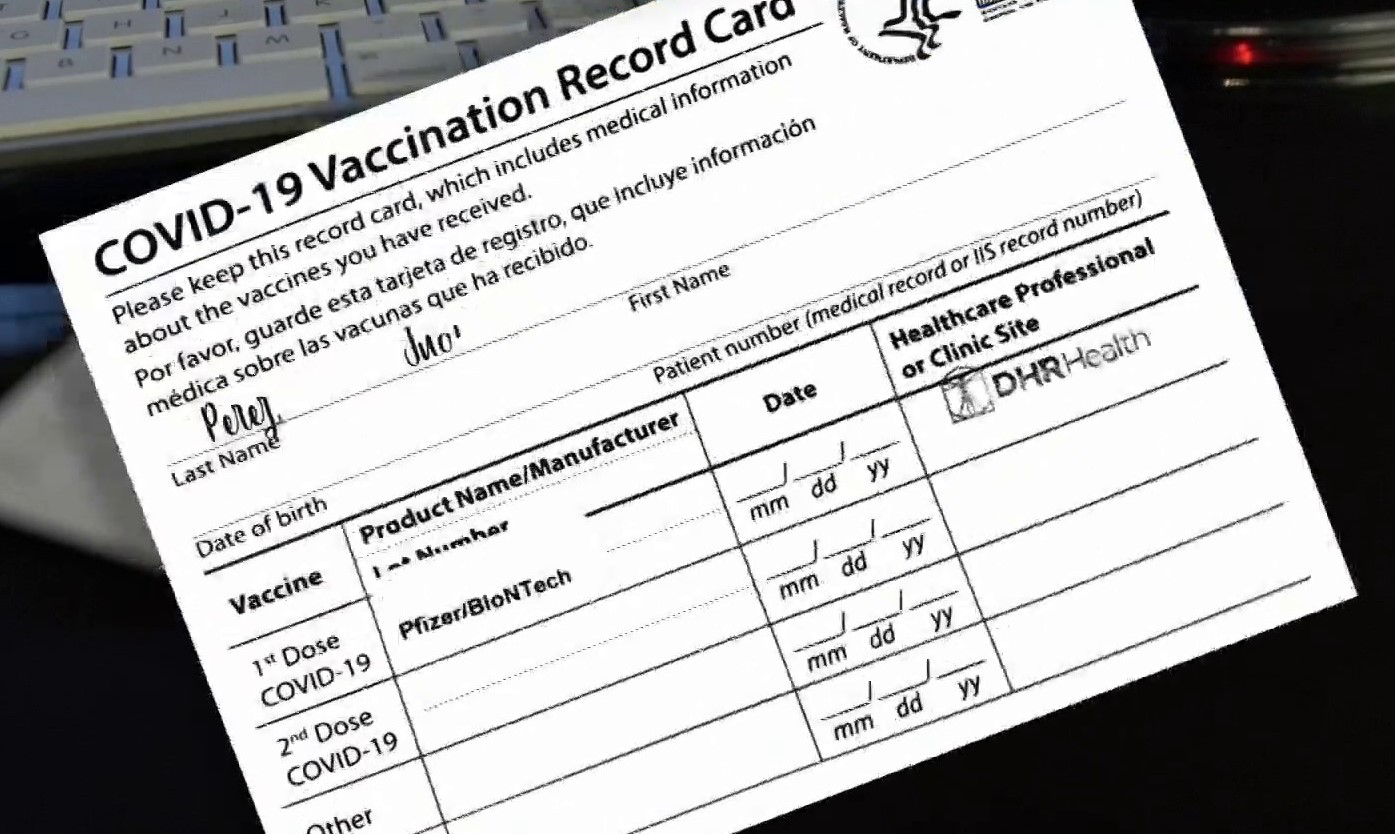
Trabajadores de una planta de Baltimore, Maryland, que fabrica dos vacunas contra el COVID-19, combinaron accidentalmente los ingredientes de los sueros hace varias semanas, arruinando alrededor de 15 millones de dosis de la de Johnson & Johnson, informó el miércoles The New York Times (NYT).
Esto habría obligado a los reguladores a retrasar la autorización de las líneas de producción de la planta.
El NYT indicó que la planta está dirigida por Emergent BioSolutions, un socio de fabricación de Johnson & Johnson y AstraZeneca. Los funcionarios federales indicaron que se trató de un error humano, agregó el diario.
Según el NYT, el error ha detenido los envíos futuros de dosis de Johnson & Johnson en los Estados Unidos mientras la Administración de Alimentos y Medicamentos (FDA, por sus siglas en inglés) investiga. Johnson & Johnson ha fortalecido su control sobre el trabajo de Emergent BioSolutions para evitar más fallas de calidad, agregó el medio de comunicación en su versión digital.
El incidente, según el NYT, no afecta las dosis de Johnson & Johnson que actualmente se administran y utilizan en todo el país. Todas esas dosis se produjeron en los Países Bajos, donde las operaciones han sido totalmente aprobadas por los reguladores federales, según el diario.
Pero todos los envíos posteriores de la vacuna de Johnson & Johnson, que se proyectaban en un total de decenas de millones de dosis en el próximo mes, provenían de la enorme planta de Baltimore, agregó el Times.
Esos envíos ahora están en duda mientras se resuelven los problemas de control de calidad, según fuentes del NYT.
Johnson & Johnson no tardó en responder mediante un comunicado de prensa sin mencionar el reporte del NYT.
"Al igual que con la fabricación de cualquier medicamento biológico complejo o vacuna, la puesta en marcha de un nuevo proceso incluye pruebas y controles de calidad para garantizar que la fabricación esté validada y que el producto final cumpla con nuestros estándares de alta calidad. Este enfoque incluye tener especialistas dedicados sobre el terreno en las empresas que forman parte de nuestra red de fabricación global para respaldar la seguridad y la calidad", dijo la farmacéutica.
"Este proceso de control de calidad identificó un lote que no cumplía con los estándares de calidad en Emergent BioSolutions, un sitio que aún no está autorizado para fabricar fármacos para nuestra vacuna contra el COVID-19. Este lote nunca avanzó a las etapas de llenado y acabado de nuestro proceso de fabricación", agregó.